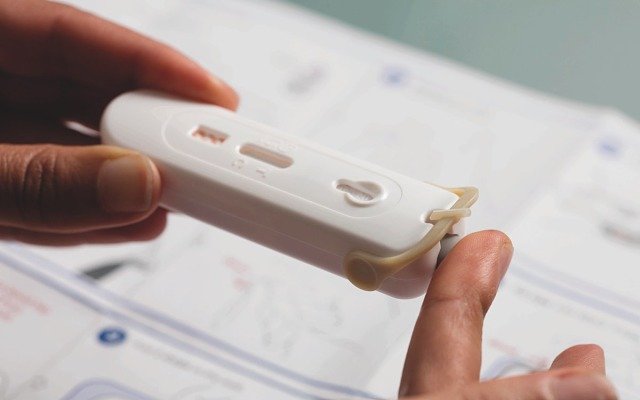
Medical device company Atomo Diagnostics (ASX: AT1) has received approval from the Therapeutic Goods Administration for its AtomoRapid (IgG/IgM) antibody test kit for patients with suspected COVID-19.
The test is able to determine if a patient has developed antibodies to the virus and can obtain results from a drop of blood within 15 minutes.
TGA approval means the kit will be added to Atomo’s existing Australian Register of Therapeutic Goods listing, alongside the Atomo HIV Self-Test screening kit.
It will then be supplied to Australian laboratories, medical practitioners and health care professionals in residential and aged care facilities.
AtomoRapid has been manufactured in collaboration with French company NG Biotech, with NG manufacturing the test strip and Atomo manufacturing the device and being the listed manufacturer.
The test kit approved by the TGA is the same as the kit which is currently being sold by NG to consumers in France.
Local market supply
Atomo co-founder and managing director John Kelly said TGA approval would provide a high-quality and reliable rapid antibody test for the local market.
“We already sell Australia’s only approved HIV self-test kit and we know that our solution simplifies rapid blood-based testing in point-of-care settings,” he said.
“We are excited that our test can now be used in our home market [of Australia] to assist in the fight against COVID-19.”
Mr Kelly said the company would look to submit AtomoRapid for assessment by the Peter Doherty Institute for Infection and Immunity at Melbourne University.
The institute has been engaged by Victoria’s Department of Health to assist with post-market validation of new COVID-19 rapid tests to inform their best use.
Independent studies
An independent study at the Hopital Bicêtre in Paris utilising Atomo’s COVID-19 test in conjunction with its Pascal rapid diagnostic testing platform used the serum from 101 patients hospitalised with coronavirus to check for antibodies of IgM (early infection response) and IgG (sustained infection response).
The tests found that sensitivity and specificity were 97.0% and 100% respectively, 15 days after the onset of symptoms.
A further study conducted using Atomo’s Galileo platform tested 78 positive and 22 negative samples collected from patients who were confirmed positive or negative for IgM and IgG, found that 15 days after the onset of symptoms sensitivity and specificity were 96.8% and 100% respectively.
Mr Kelly said the results of the studies on Atomo’s Pascal and Galileo devices indicated materially-equivalent results with both demonstrating 100% specificity.
Commercial opportunities
Prior to TGA approval, Atomo held preliminary discussions to assess Australian commercial distribution channels for AtomoRapid.
Mr Kelly said the company would now engage across segments where it believes COVID-19 antibody testing has a significant role to play, including public health providers, corporate occupational health and safety, and aged care.
“We see strong potential for use of our test across a number of channels and we believe TGA approval will accelerate these opportunities,” he said.
“Performance data generated from the French studies and Atomo’s proven ease-of-use in the field make our test well-suited for deployment in a large country such as Australia with a variety of point-of-care settings.”
He said any commercial relationships in Australia would add to Atomo’s current revenue-accretive supply agreements for COVID-19 testing with offshore partners Access Bio (covering the US and Korean markets) and NG Biotech (France).
With the majority of current production committed under existing contracts, an initial allocation of 100,000 units has been allocated to the Australian market, to be scaled up based on demand.